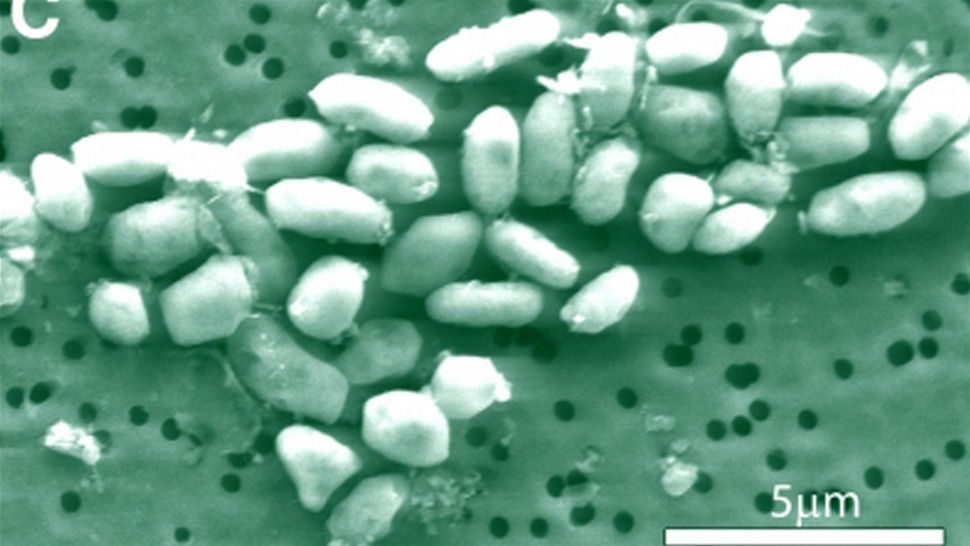
 Podobné titulky oznamovaly minulý týden objev amerických badatelů, kteří v kalifornském jezeře Mono Lake nalezli bakterie, které jsou schopny zabudovávat do svých makromolekulárních komponent (DNA, proteinů) namísto obvyklého fosforu arzén, který je pro naprostou většinu organismů toxický.
Podobné titulky oznamovaly minulý týden objev amerických badatelů, kteří v kalifornském jezeře Mono Lake nalezli bakterie, které jsou schopny zabudovávat do svých makromolekulárních komponent (DNA, proteinů) namísto obvyklého fosforu arzén, který je pro naprostou většinu organismů toxický.
Na rozdíl od novinářů a některých nepříliš seriózních vědců si myslím, že se žádná velká senzace nekoná.
Ty kalifornské bakterie jsou skutečně velmi zajímavé a unikátní organizmy, avšak jejich objevení žádným radikálním průlomem není. Sloučeniny fosforu jsou podobné sloučeninám arzénu, který jsou však pro běžné buňky jedovaté. Když se buňky pokusí sloučeniny arzénu (zvláště arzeničnany resp. arzenáty) použít namísto fosfátů, odumřou, protože enzymy a jiné biologické makromolekuly, do kterých se zabuduje místo fosforu arzén, se rychle rozkládají a jsou nefunkční.
Nově objevené akterie se s tímto problémem dokázaly zřejmě nějak vypořádat, a bude neobyčejně zajímavé zjistit biochemické detaily toho, jak to dělají.
Ale – i tyto nově objevené bakterie mají raději fosfor než arzén, který používají spíše „z nouze“.
Mimochodem, už dávno jsou známy bakterie jiným způsobem také „žijící z arzénu“ – získávají totiž energii oxidací živin spřaženou s redukcí arzeničnanů na arzenitany (podobně jako my získáváme energii oxidací živin spřaženou s redukcí molekul kyslíku).
Novináři také vznášeli otázku, jesti je pravděpodobné, že mimo Zemi existuje život založený na jiných chemických principech, než ten pozemský.
Na to lze asi odpovědět velmi stručně – nevíme…
My toho prostě víme opravdu hrozně málo. Uvědomme si, že v naší galaxii je cca 100 miliard hvězd a ve vesmíru více než 100 miliard galaxií. A my víme něco málo o tom, co existuje na jedné planetě poblíž jedné z těch kvadrilionů hvězd. a mnoha planetách jsou pravděpodobně organismy, které si ani nedokážeme představit. Osobně si myslím, že život existuje na mnoha místech vesmíru a že se asi zakládá na podobných chemických principech, jako na Zemi, tedy na bázi sloučenin uhlíku, kyslíku a dusíku.
Prozatím nic nesvědčí ani o tom, že by na Zemi existoval nějaký „alternativní“ život, který by např. používal k zápisu genetické informace něco jiného než nukleové kyseliny a jako základní stavební a funkční molekuly něco jiného než proteiny (bílkoviny) složené z aminokyselin.
Nově objevené bakterie jsou především dalším příkladem toho, jak se život umí přizpůsobit extrémním podmínkám. Dalšími známými příklady jsou organizmy žijící v extrémních teplotách (i nad 100oC) (termofily), ve vysokých koncentracích solí (halofily) nebo téměř neprozkoumané bakterie vyskytující se v horninách velmi hluboko pod zemí.
To, že základní chemické principy všeho pozemského živého, od nejjednodušších bakterií až po obratlovce, jsou v podstatě shodné, ukazuje, že pozemský život pochází nepochybně z jediného dávného prapředka.
Je ale třeba poctivě říci, že dnes nevíme jak život na Zemi před cca 4 miliardami let vznikl, i když existuje řada rozumných teorií i zajímavých experimentálních výsledků.
Život ale docela dobře mohl vzniknout někde jinde ve vesmíru a na Zemi nějak připutovat (na což bych si docela vsadil).
Prozatím o tom můžeme jen spekulovat, ale možná za nějakých pouhých tisíc let to třeba už budeme vědět…
Níže přetiskuji pro zájemce článek z časopisu Science, který komentuje onen objev „arzénových bakterií“.
******************************************************
What Poison? Bacterium Uses Arsenic to Build DNA and Other Molecules
Elizabeth Pennisi
From elephants to the bacterium Escherichia coli, all forms of life on Earth depend on the same six elements: oxygen, carbon, hydrogen, nitrogen, phosphorus, and sulfur. “The paradigm is that the chemistry of life is so specific that any change in chemistry also changes molecular stability and reactivity, which would not be tolerated,” says Clara Chan, a geomicrobiologist at the University of Delaware, Newark.
In a paper published online by Science (www.sciencemag.org/cgi/content/abstract/science.1197258) this week, however, an exception to that rule makes a surprising debut. Meet GFAJ-1, a bacterial strain that researchers say can replace the phosphorus in its key biomolecules, including DNA, with the legendary poison arsenic. “This is a very impressive and exciting discovery,” says Barry Rosen, a biochemist at Florida International University in Miami. “The implication of this work is that life can be quite different from what we know,” agrees Chan.
In 2009, Felisa Wolfe-Simon, a geomicrobiologist based at the U.S. Geological Survey in Menlo Park, California, and two colleagues argued that arsenic could have stood in for phosphorus in ancient living systems. Phosphorus, in the form of the compound phosphate, forms the backbone of strands of DNA and RNA, as well as ATP and NAD, two molecules key to energy transfer in a cell. Arsenic, Wolfe-Simon pointed out, sits just below phosphorus on the periodic table and has similar chemical properties. Indeed, its toxicity to people and most forms of life arises when cells try to use arsenic in lieu of phosphorus.
Despite that, Wolfe-Simon speculated that some microbes might be able to adapt to using arsenic. Others were skeptical. The arsenic-containing compound arsenate is much more unstable than phosphate in water, and no cell would be able to cope with that, critics argued.
To test her hypothesis, Wolfe-Simon collected mud from Mono Lake, California, a desert body of water known for having high arsenic levels, and grew the microorganisms from it in increasing concentrations of arsenate. She didn’t add any phosphate or other phosphorus-containing compounds to the growth medium, as is typically done to sustain microbes. Instead, she periodically transferred the growing cultures to a new dish to reduce the concentration of any original phosphorus to the point that any microbe making new DNA or other biomolecules would need to use the arsenic to survive.
Like others, says Wolfe-Simon, she didn’t really expect to find any survivors. So she was thrilled and surprised when one evening she checked the latest cultures under the microscope and saw fast-moving bacteria. She rechecked the components of the culture media to confirm there were no phosphorus contaminants. She and her colleagues then began to subject the microbes to sophisticated analyses to see if arsenic had been utilized by the bacteria. “I held my breath with every one,” says Wolfe-Simon.
One form of mass spectrometry showed that the arsenic was inside the bacterial cells and not some impurity sticking to the outside of the cell. When the researchers added radioactively labeled arsenate to the bacteria’s culture, they were later able to discern its presence in the protein, lipid, nucleic acid, and metabolite fractions of the cells, suggesting that arsenic had been incorporated in molecules forming each fraction. They also separated out the DNA from the bacteria and analyzed its composition using a technique called high-resolution secondary ion mass spectrometry; the isolated DNA contained arsenic.
Tests utilizing the intense x-rays at a synchrotron facility offered additional support, indicating that at least some of the arsenic in the bacteria was in the form of arsenate with the appropriate molecular bonds to carbon and oxygen atoms to replace the phosphates in DNA and other molecules.
Such work has convinced many that Wolfe-Simon’s team has isolated a bacterium that uses arsenic to grow. “The organization of the experiments presents convincing and exhaustive results,” says Milva Pepi, an environmental microbiologist at the University of Siena in Italy. But not everyone agrees. Rosen finds the study “believable” but says he still has lingering concerns that the arsenic is simply concentrated in the bacterial cell’s extensive vacuoles and not incorporated into its biochemistry. He would like to see Wolfe-Simon’s team demonstrate a functional arsenic-containing enzyme, for example. Steven Benner, an astrobiologist at the Foundation for Applied Molecular Evolution in Gainesville, Florida, is more skeptical: That GFAJ-1 uses arsenic as a replacement for phosphorus, “is, in my opinion, not established by this work,” he says.
Wolfe-Simon isn’t arguing that GFAJ-1 prefers, or even naturally uses, arsenic. Mono Lake has a lot of phosphorus as well as arsenic, and the strain grows better when supplied with phosphorus. But to her and others, GFAJ-1 is proof that phosphorus-free life forms can exist and may do so somewhere on Earth. Next, Wolfe-Simon wants to collect samples from places with high arsenic but low phosphorus concentrations in hopes of finding microbes that depend solely on the former.
Wolfe-Simon speculates that organisms like GFAJ-1 could have thrived in the arsenic-laden hydrothermal vent–like environments of early Earth, where some researchers think life first arose, and that later organisms may have adapted to using phosphorus. Others say they’ll refrain from such speculation until they see more evidence of GFAJ-1’s taste for arsenic and understand how the DNA and other biomolecules can still function with the element incorporated. “As in this type of game changer, some people will rightly want more proof,” says microbiologist Robert Gunsalus of the University of California, Los Angeles. “There is much to do in order to firmly put this microbe on the biological map.”
Převzato z blogu autora na Aktuálně
Foto: zdroj

